El ácido más utilizado en las fábricas de estampación y teñido: el ácido acético.
El ácido acético (fórmula química CH3COOH), comúnmente conocido como ácido acético, es un ácido monobásico orgánico. El ácido acético con un contenido del 98% se congela a bajas temperaturas y se conoce comúnmente como ácido acético glacial. El valor de pH de una solución acuosa de 1 mol/L de ácido acético (equivalente a la concentración de vinagre) es 2,4.
El ácido acético debe ser el ácido más utilizado en los procesos de impresión y teñido: neutralización ácida del pretratamiento alcalino, ajuste del pH de tintes dispersos, tintes ácidos, tintes catiónicos, etc., ajuste del pH del pulido de celulasa ácida, etc.
1. Efecto del ácido sobre la fibra de algodón.
1. El ácido puede hacer que disminuya la resistencia de la fibra de algodón. La celulosa del algodón se hidrolizará cuando encuentre ácido. El principio es el siguiente: los residuos de glucosa de las macromoléculas de celulosa están conectados por enlaces 1,4-glicosídicos y los enlaces glicosídicos son muy sensibles al ácido. La celulosa del algodón se hidroliza cuando se encuentra con ácido. Cuando se rompen todos los enlaces glicosídicos de la macromolécula de celulosa, se genera glucosa. Después de hidrolizar la celulosa, se genera celulosa hidrolizada, el grado de polimerización disminuye y la resistencia también disminuye. Por lo tanto, el ácido puede hacer que disminuya la resistencia de la fibra de algodón.
2. La influencia de diferentes ácidos sobre la resistencia de las fibras de algodón:
Como se muestra en la figura anterior, el ácido clorhídrico y el ácido nítrico tienen el mayor impacto en la reducción de la resistencia de las fibras de algodón, seguidos por el ácido sulfúrico, luego el bisulfato de sodio y el ácido fosfórico. El ácido fórmico tiene una reducción de fuerza mucho mayor que el ácido acético, pero muchas fábricas de teñido todavía usan ácido fórmico para la neutralización del ácido, probablemente porque el costo del ácido fórmico es menor que el del ácido acético. Teniendo en cuenta todos los factores, el ácido acético es el ácido más adecuado para el procesamiento de fibra de algodón.
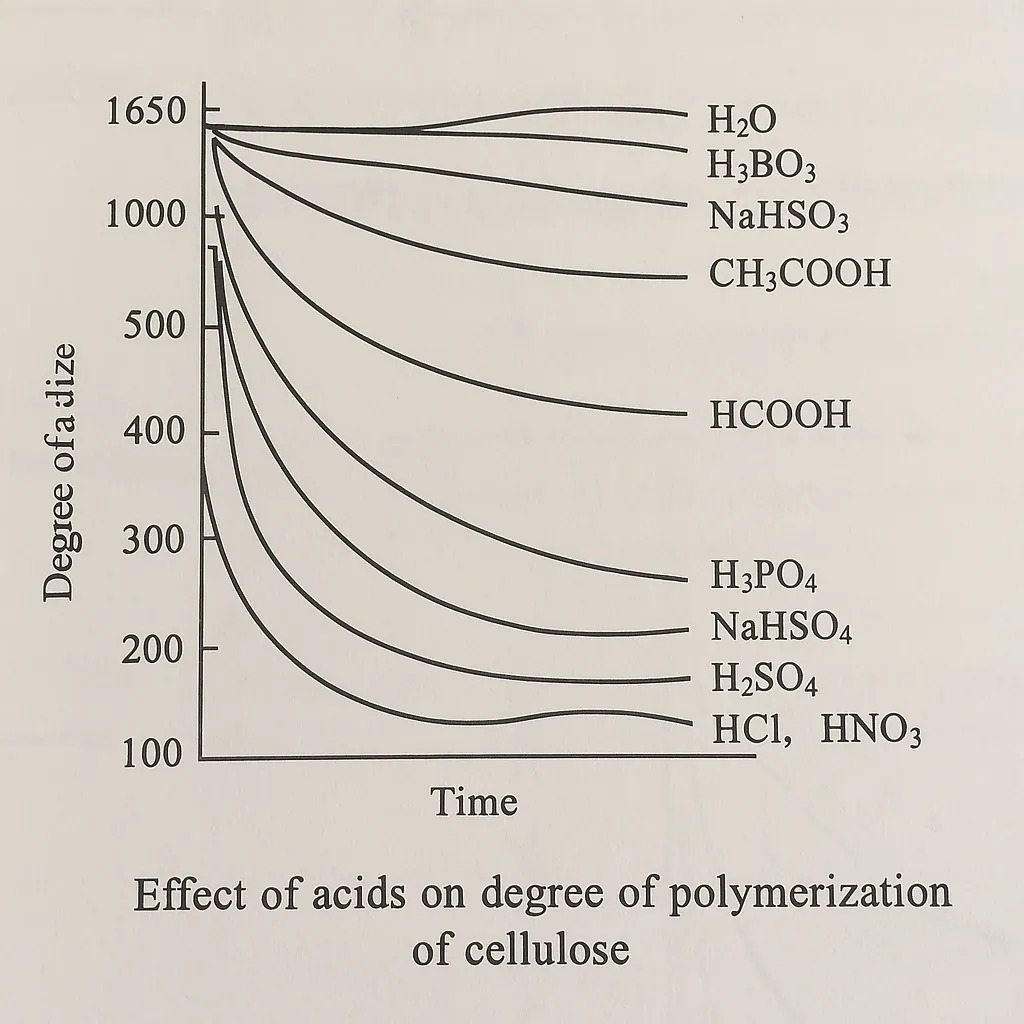
Como se muestra en la figura anterior, el ácido clorhídrico y el ácido nítrico tienen el mayor impacto en la reducción de la resistencia de las fibras de algodón, seguidos por el ácido sulfúrico, luego el bisulfato de sodio y el ácido fosfórico. El ácido fórmico tiene una reducción de fuerza mucho mayor que el ácido acético, pero muchas fábricas de teñido todavía usan ácido fórmico para la neutralización del ácido, probablemente porque el costo del ácido fórmico es menor que el del ácido acético. Teniendo en cuenta todos los factores, el ácido acético es el ácido más adecuado para el procesamiento de fibra de algodón.
2. Sistema tampón de pH de ácido acético y acetato de sodio
Solución tampón: una solución mixta compuesta de ácido débil y su sal, base débil y su sal, que puede compensar y reducir la influencia del ácido fuerte externo o la base fuerte en el valor del pH de la solución hasta cierto punto, manteniendo así el valor del pH de la solución relativamente estable.
Al teñir tintes dispersos, tintes ácidos, tintes catiónicos y otros tintes, el pH es generalmente ácido. Para lograr un control de pH estable, algunas fábricas utilizarán un sistema tampón de ácido acético y acetato de sodio para controlar con precisión el pH y mejorar la reproducibilidad y la tasa de éxito del teñido.
La siguiente es la preparación de una solución tampón de ácido acético y acetato de sodio con el pH de uso común:
Tampón de ácido acético y acetato de sodio (pH 3,6)
Tome 5,1 g de acetato de sodio, agregue 20 ml de ácido acético glacial y luego diluya con agua hasta 250 ml.
Tampón de ácido acético y acetato de sodio (pH 3,7)
Tome 20 g de acetato de sodio anhidro, agregue 300 ml de agua para disolver, agregue 1 ml de indicador azul de bromofenol y 60-80 ml de ácido acético glacial hasta que la solución cambie de azul a verde puro, luego diluya a 1000 ml con agua.
Tampón de ácido acético y acetato de sodio (pH 3,8)
Tome 13 ml de solución de acetato de sodio de 2 mol/L y 87 ml de solución de ácido acético de 2 mol/L, agregue 0,5 ml de solución de sulfato de cobre que contenga 1 mg de cobre por 1 ml, luego diluya a 1000 ml con agua.
Tampón de ácido acético y acetato de sodio (pH 4,5)
Tomar 18 g de acetato de sodio, añadir 9,8 ml de ácido acético glacial y luego diluir a 1000 ml con agua.
Tampón de ácido acético y acetato de sodio (pH 4,6)
Tome 5,4 g de acetato de sodio, agregue 50 ml de agua para disolver, ajuste el valor de pH a 4,6 con ácido acético glacial y luego diluya con agua a 100 ml.
Tampón de ácido acético y acetato de sodio (pH 6,0)
Tome 54,6 g de acetato de sodio, agregue 20 ml de solución de ácido acético de 1 mol/l para disolver y luego diluya con agua hasta 500 ml.
3. Ventajas del ácido acético en el pulido de celulasas
El pulido de telas de algodón se utiliza ahora ampliamente. La celulasa puede eliminar la vellosidad y las pequeñas bolitas en la superficie de las fibras de algodón. Las ventajas del ácido acético en el pulido son: debido a que el ácido acético generará acetato de sodio cuando se encuentra con sustancias alcalinas, la superficie de las fibras de algodón alcanza el valor de pH requerido durante el proceso de ajuste del pH, y debido a que el acetato de sodio se genera cuando se neutraliza el álcali dentro de la fibra, el valor de pH dentro de la fibra será mayor, por lo que ayuda a proteger la resistencia de la fibra mientras se logra el efecto de pulido de la superficie.
4. Desventajas de utilizar ácido acético para el último ajuste del pH
El estándar de seguridad de pH actual para textiles generalmente requiere 4-7,5, que es básicamente neutro y débilmente ácido, y el método de prueba es principalmente extracción. Cuando se utiliza ácido acético para el último ajuste del pH de los textiles, debido a la formación de un sistema tampón de ácido acético y acetato de sodio, el álcali dentro de la fibra no puede neutralizarse por completo. El pH de la superficie de la tela analizada con papel medidor de pH es ácido y el método de extracción a menudo muestra que el pH es alto. Por lo tanto, vale la pena ajustar el último pH. Muchas fábricas optan por utilizar ácido cítrico u otros ácidos orgánicos con una acidez más fuerte en lugar de ácido acético.










